Química Orgánica. Introducción
- Red Cientifica Escolar
- 9 jul 2024
- 5 Min. de lectura
Actualizado: 10 jul 2024
En esta guía de lectura vamos a presentar un breve resumen de las propiedades y nomenclatura de los hidrocarburos y sus principales familias.
Reseña Histórica del Estudio de la Química Orgánica
La química orgánica es una rama de la química que se centra en el estudio de los compuestos que contienen carbono. Su desarrollo ha sido fundamental para avances en medicina, agricultura, y tecnología. Aquí te presento un breve recorrido por su historia.
Siglo XVIII - Comienzos:
En los siglos XVIII y XIX, la química se centraba principalmente en compuestos inorgánicos. Se creía que los compuestos orgánicos, que se encuentran en seres vivos, solo podían ser sintetizados por organismos vivos debido a una "fuerza vital". Este concepto se conocía como vitalismo.
1807 - Berzelius y la Nomenclatura:
Jöns Jacob Berzelius, un químico sueco, propuso una nomenclatura para los compuestos orgánicos e inorgánicos, lo que ayudó a sistematizar la química. También introdujo términos como "polímeros" y "isómeros", fundamentales para la química orgánica.
1828 - Síntesis de la Urea:
El paradigma del vitalismo comenzó a desmoronarse en 1828, cuando el químico alemán Friedrich Wöhler sintetizó urea (un compuesto orgánico) a partir de cianato de amonio (un compuesto inorgánico). Este experimento demostró que los compuestos orgánicos podían ser creados a partir de compuestos inorgánicos, desafiando la idea de la fuerza vital.
(Timberlake, 2013)
Siglo XIX - Avances en la Estructura Molecular:
Durante el siglo XIX, químicos como August Kekulé y Archibald Scott Couper propusieron la teoría estructural, que describía cómo los átomos de carbono se unen para formar estructuras tridimensionales. Kekulé es famoso por proponer la estructura cíclica del benceno, un descubrimiento crucial para entender la química de los compuestos aromáticos.
Siglo XX - Explosión de Descubrimientos:
El siglo XX vio un auge en la química orgánica, con descubrimientos que impactaron profundamente diversas industrias. La creación de polímeros como el nylon y el polietileno revolucionó la industria de los plásticos. En el ámbito farmacéutico, la síntesis de compuestos como la penicilina y otros antibióticos salvó innumerables vidas.
Actualidad - Química Orgánica Moderna:
Hoy en día, la química orgánica sigue evolucionando, con avances en la síntesis de compuestos complejos y el desarrollo de nuevos materiales y medicamentos. La química verde, que busca procesos químicos más amigables con el medio ambiente, y la química computacional, que utiliza computadoras para modelar reacciones químicas, son áreas emergentes que prometen revolucionar aún más esta fascinante disciplina.
En resumen, la química orgánica ha recorrido un largo camino desde sus inicios, transformándose en una ciencia crucial que continúa impactando nuestras vidas de maneras profundas y diversas.
Hidrocarburos y la Química del Carbono
Hidrocarburos:
Los hidrocarburos son compuestos químicos formados únicamente por átomos de carbono (C) e hidrógeno (H). Son la base de la química orgánica y se dividen en varias categorías según su estructura y tipo de enlaces entre los átomos de carbono:
Alcanos:
Son hidrocarburos saturados, es decir, contienen solo enlaces simples entre los átomos de carbono. Su fórmula general es CₙH₂ₙ₊₂. Ejemplo: metano (CH₄).
Alquenos:
Son hidrocarburos insaturados con al menos un doble enlace carbono-carbono. Su fórmula general es CₙH₂ₙ. Ejemplo: etileno (C₂H₄).
Alquinos:
Son hidrocarburos insaturados con al menos un triple enlace carbono-carbono. Su fórmula general es CₙH₂ₙ₋₂. Ejemplo: acetileno (C₂H₂).
Aromáticos:
Son hidrocarburos que contienen uno o más anillos bencénicos, que son estructuras cíclicas con enlaces dobles y simples alternados. Ejemplo: benceno (C₆H₆).
Química del Carbono:
El carbono es un elemento único y fundamental en la química orgánica debido a su capacidad para formar cuatro enlaces covalentes con otros átomos, incluyendo otros átomos de carbono. Esta propiedad permite la formación de una gran variedad de estructuras, desde cadenas lineales y ramificadas hasta anillos y estructuras tridimensionales complejas.
Debido a su configuración electrónica, el Carbono presenta 4 electrones de valencia, y debido a la hibridación de orbitales, el Carbono puede formar 4 enlaces simples, o 2 enlaces dobles, o 2 enlaces simples y 1 doble, o 1 simple y 1 triple.
Cadenas Carbonadas:
Los átomos de carbono pueden unirse en cadenas de diferentes longitudes y formas, lo que da lugar a una variedad casi infinita de compuestos orgánicos.
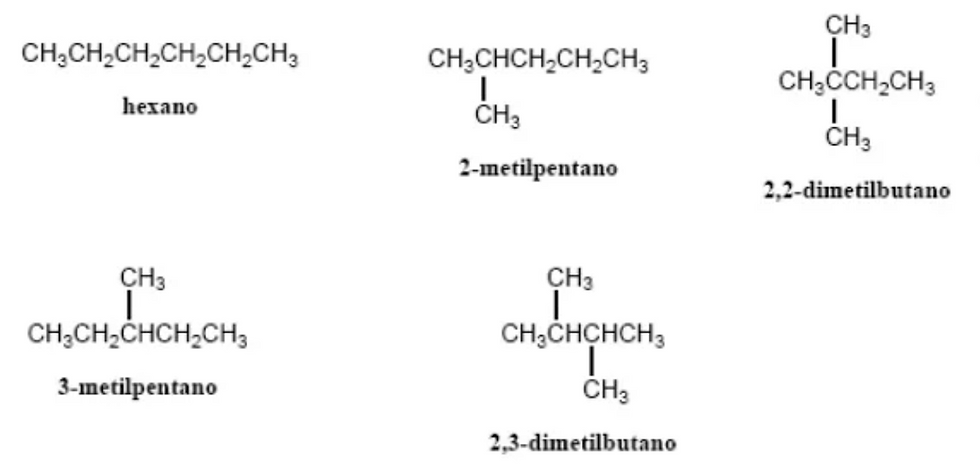
Isomería:
El carbono puede formar compuestos con la misma fórmula molecular pero diferentes estructuras, conocidos como isómeros. Los isómeros pueden tener propiedades físicas y químicas muy distintas.
Grupos Funcionales:
La presencia de diferentes grupos funcionales (como -OH, -NH_2, -COOH) en las moléculas orgánicas determina su reactividad y propiedades químicas. Los grupos funcionales son específicos conjuntos de átomos dentro de una molécula que tienen un comportamiento químico característico. Para profundizar, puedes revisar nuestro artículo Grupos Funcionales. Reconocimiento y Nomenclatura.
Reacciones Orgánicas:
La química del carbono incluye una amplia gama de reacciones, como la combustión, halogenación, polimerización, y muchas más. Estas reacciones son fundamentales para la síntesis de nuevos compuestos y materiales.
En resumen, los hidrocarburos y la química del carbono son la base de la química orgánica, permitiendo la formación y manipulación de una inmensa diversidad de compuestos que son esenciales para la vida y la industria.
Fórmulas estructurales
Una molécula puede representarse mediante su fórmula química, pero ésta no nos informa sobre la disposición de los átomos en el espacio. Por ejemplo, una molécula de hexano puede representarse de muchas formas: fórmula molecular, modelo de barras y esferas, fórmula estructural expandida, fórmula estructural condensada y fórmula esquelética.
Puedes revisar en detalle todas las formas de representación en química en el artículo correspondiente.
Guía de Nomenclatura Orgánica para Hidrocarburos
La nomenclatura orgánica es un sistema de nombres utilizados para describir las estructuras de los compuestos orgánicos. Aquí se presenta una guía precisa y completa para la nomenclatura de los principales grupos de hidrocarburos: alcanos, alquenos, alquinos y compuestos aromáticos.
Alcanos
Estructura General: Los alcanos son hidrocarburos saturados con enlaces simples C-C y tienen la fórmula general CₙH₂ₙ₊₂.
Reglas de Nomenclatura:
Identificar la cadena principal: La cadena más larga continua de átomos de carbono.
Numerar la cadena principal: Numerar los átomos de carbono en la cadena principal desde el extremo más cercano a la primera ramificación.
Nombrar las sustituciones: Identificar y nombrar los grupos alquilo (ramificaciones) unidos a la cadena principal.
Escribir el nombre completo: Enumerar los sustituyentes en orden alfabético, precedidos por su posición en la cadena principal, seguida del nombre del alcano correspondiente.
Ejemplo:
CH₃-CH₂-CH₃: Propano
CH₃-CH(CH₃)-CH₃: 2-Metilpropano
Lista de Prefijos para la Longitud de la Cadena:
1 C: Met-
2 C: Et-
3 C: Prop-
4 C: But-
5 C: Pent-
6 C: Hex-
7 C: Hept-
8 C: Oct-
9 C: Non-
10 C: Dec-
Alquenos
Estructura General: Los alquenos son hidrocarburos insaturados con uno o más dobles enlaces C=C y tienen la fórmula general CₙH₂ₙ.
Reglas de Nomenclatura:
Identificar la cadena principal: La cadena más larga que contiene el doble enlace.
Numerar la cadena principal: Numerar los átomos de carbono desde el extremo más cercano al doble enlace.
Indicar la posición del doble enlace: Escribir la posición del primer átomo de carbono del doble enlace.
Nombrar los sustituyentes: Identificar y nombrar los grupos alquilo unidos a la cadena principal.
Escribir el nombre completo: Indicar la posición del doble enlace antes del nombre del alqueno correspondiente.
Ejemplo:
CH₂=CH₂: Eteno
CH₂=CH-CH₃: Propeno
CH₂=CH-CH₂-CH₃: 1-Buteno
CH₃-CH=CH-CH₃: 2-Buteno
Alquinos
Estructura General: Los alquinos son hidrocarburos insaturados con uno o más triples enlaces C≡C y tienen la fórmula general CₙH₂ₙ₋₂.
Reglas de Nomenclatura:
Identificar la cadena principal: La cadena más larga que contiene el triple enlace.
Numerar la cadena principal: Numerar los átomos de carbono desde el extremo más cercano al triple enlace.
Indicar la posición del triple enlace: Escribir la posición del primer átomo de carbono del triple enlace.
Nombrar los sustituyentes: Identificar y nombrar los grupos alquilo unidos a la cadena principal.
Escribir el nombre completo: Indicar la posición del triple enlace antes del nombre del alquino correspondiente.
Ejemplo:
CH≡CH: Etino
CH≡C-CH₃: Propino
CH₃-C≡C-CH₃: 2-Butino
Compuestos Aromáticos
Estructura General: Los compuestos aromáticos contienen anillos de benceno, que son estructuras cíclicas con enlaces dobles y simples alternados.
Reglas de Nomenclatura:
Benceno como base: Usar "benceno" como el nombre base.
Numerar el anillo: Numerar los átomos de carbono en el anillo de benceno, comenzando por el sustituyente más importante.
Nombrar los sustituyentes: Identificar y nombrar los grupos unidos al anillo de benceno.
Escribir el nombre completo: Indicar la posición de los sustituyentes antes del nombre del benceno.
Ejemplo:
C₆H₆: Benceno
C₆H₅-CH₃: Metilbenceno (Tolueno)
C₆H₄(CH₃)₂: 1,2-Dimetilbenceno (Ortoxileno)
Ejercicios
Referencias
Whitten, K., Davis, R., Peck, L., & Stanley, G. (2015). Quimica (Décima edición). Cengagte Learning Editores.
Timberlake, K. C. (2013). Química General, Orgánica y Biológica: Estructuras de la vida (Cuarta edición). Pearson Educación de México.















Comentarios